පෙප්ටයිඩ යනු පෙප්ටයිඩ බන්ධන හරහා බහු ඇමයිනෝ අම්ල සම්බන්ධ වීමෙන් සෑදෙන සංයෝග කාණ්ඩයකි.ඒවා සජීවී ජීවීන් තුළ බහුලව දක්නට ලැබේ.මේ දක්වා, ජීවී ජීවීන් තුළ පෙප්ටයිඩ දස දහස් ගණනක් සොයාගෙන ඇත.විවිධ පද්ධති, අවයව, පටක සහ සෛලවල ක්රියාකාරී ක්රියාකාරකම් නියාමනය කිරීමේදී සහ ජීව ක්රියාකාරකම් වලදී පෙප්ටයිඩ වැදගත් කාර්යභාරයක් ඉටු කරන අතර බොහෝ විට ක්රියාකාරී විශ්ලේෂණය, ප්රතිදේහ පර්යේෂණ, ඖෂධ සංවර්ධනය සහ වෙනත් ක්ෂේත්ර සඳහා භාවිතා වේ.ජෛව තාක්ෂණය සහ පෙප්ටයිඩ සංස්ලේෂණ තාක්ෂණයේ දියුණුවත් සමඟ, වැඩි වැඩියෙන් පෙප්ටයිඩ ඖෂධ සායනයෙහි සංවර්ධනය කර යොදවා ඇත.
පෙප්ටයිඩ වෙනස් කිරීම් රාශියක් ඇත, ඒවා සරලව පශ්චාත් වෙනස් කිරීම සහ ක්රියාවලි වෙනස් කිරීම (ව්යුත්පන්න ඇමයිනෝ අම්ල වෙනස් කිරීම භාවිතා කිරීම) සහ N-පර්යන්ත වෙනස් කිරීම, C-පර්යන්ත වෙනස් කිරීම, පැති දාම වෙනස් කිරීම, ඇමයිනෝ අම්ල වෙනස් කිරීම, ඇටසැකිල්ල වෙනස් කිරීම ලෙස බෙදිය හැකිය. ආදිය, වෙනස් කිරීමේ අඩවිය මත පදනම්ව (රූපය 1).පෙප්ටයිඩ දාමවල ප්රධාන දාම ව්යුහය හෝ පැති දාම කණ්ඩායම් වෙනස් කිරීමට වැදගත් මාධ්යයක් ලෙස, පෙප්ටයිඩ වෙනස් කිරීම මගින් පෙප්ටයිඩ සංයෝගවල භෞතික හා රසායනික ගුණාංග ඵලදායී ලෙස වෙනස් කළ හැකිය, ජල ද්රාව්යතාව වැඩි කරයි, vivo හි ක්රියාකාරී කාලය දිගු කරයි, ඒවායේ ජීව විද්යාත්මක ව්යාප්තිය වෙනස් කරයි, ප්රතිශක්තිකරණ භාවය ඉවත් කරයි. , විෂ සහිත අතුරු ආබාධ අඩු කිරීම යනාදිය මෙම ලිපියේ ප්රධාන පෙප්ටයිඩ වෙනස් කිරීමේ උපාය මාර්ග කිහිපයක් සහ ඒවායේ ලක්ෂණ හඳුන්වා දී ඇත.
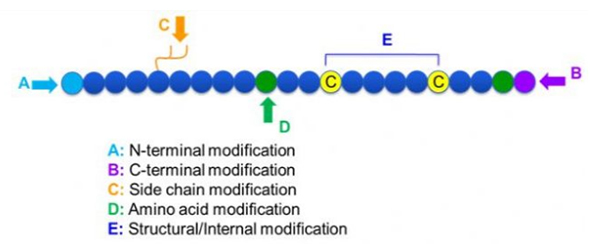
1. චක්රීයකරණය
චක්රීය පෙප්ටයිඩ ජෛව වෛද්ය විද්යාවේ බොහෝ යෙදුම් ඇති අතර ජීව විද්යාත්මක ක්රියාකාරකම් සහිත බොහෝ ස්වාභාවික පෙප්ටයිඩ චක්රීය පෙප්ටයිඩ වේ.චක්රීය පෙප්ටයිඩ රේඛීය පෙප්ටයිඩවලට වඩා දෘඩ වීමට නැඹුරු වන බැවින්, ඒවා ආහාර ජීර්ණ පද්ධතියට අතිශයින් ප්රතිරෝධී වන අතර, ආහාර ජීර්ණ පත්රයේ නොනැසී පැවතිය හැකි අතර ඉලක්කගත ප්රතිග්රාහක සඳහා ප්රබල බැඳීමක් පෙන්නුම් කරයි.විශේෂයෙන් විශාල ව්යුහාත්මක ඇටසැකිල්ලක් සහිත පෙප්ටයිඩ සඳහා චක්රීය පෙප්ටයිඩ සංස්ලේෂණය කිරීමට වඩාත්ම සෘජු ක්රමය චක්රීයකරණයයි.චක්රීයකරණ මාදිලියට අනුව, එය පැති දාම-පැති දාම වර්ගය, පර්යන්ත - පැති දාම වර්ගය, පර්යන්තය - පර්යන්ත වර්ගය (අවසානයේ සිට අවසානය දක්වා) ලෙස බෙදිය හැකිය.
(1) පැති දාමය-පැති දාමය
පැති දාමයේ සිට පැති දාම චක්රීයකරණයේ වඩාත් සුලභ වර්ගය වන්නේ සයිස්ටීන් අවශේෂ අතර ඩයිසල්ෆයිඩ් පාලමයි.මෙම චක්රීයකරණය හඳුන්වා දෙනු ලබන්නේ සිස්ටීන් අපද්රව්ය යුගලයක් මගින් ආරක්ෂා කර පසුව ඔක්සිකරණය වී ඩයිසල්ෆයිඩ් බන්ධන සෑදීමෙනි.සල්ෆයිඩ්රයිල් ආරක්ෂණ කන්ඩායම් වරණාත්මකව ඉවත් කිරීම මගින් බහු චක්රීය සංශ්ලේෂණය ලබා ගත හැක.චක්රීයකරණය පශ්චාත් විඝටන ද්රාවකයක් හෝ පෙර විඝටන දුම්මලයක් මත සිදු කළ හැක.දුම්මල මත චක්රීයකරණය ද්රාව්ය චක්රීකරණයට වඩා අඩු ඵලදායී විය හැක, මන්ද දුම්මල මත ඇති පෙප්ටයිඩ පහසුවෙන් චක්රීය අනුකූලතා ඇති නොකරයි.තවත් ආකාරයක පැති දාම - පැති දාම චක්රීයකරණය යනු ඇස්පාර්ටික් අම්ලය හෝ ග්ලූටමික් අම්ල අපද්රව්ය සහ මූලික ඇමයිනෝ අම්ලය අතර ඇමයිඩ ව්යුහයක් සෑදීමයි, ඒ සඳහා පැති දාම ආරක්ෂණ කණ්ඩායම පොලිපෙප්ටයිඩයෙන් තෝරා බේරා ඉවත් කිරීමට හැකි විය යුතුය. දුම්මල මත හෝ විඝටනය වීමෙන් පසුව.තුන්වන ආකාරයේ පැති දාම - පැති දාම චක්රීයකරණය යනු ටයිරොසීන් හෝ p-හයිඩ්රොක්සිෆෙනයිල්ග්ලයිසීන් මගින් ඩයිපීනයිල් ඊතර් සෑදීමයි.ස්වභාවික නිෂ්පාදනවල මෙම වර්ගයේ චක්රීයකරණය ක්ෂුද්රජීවී නිෂ්පාදනවල පමණක් දක්නට ලැබෙන අතර සයිකල්කරණ නිෂ්පාදන බොහෝ විට විභව ඖෂධීය වටිනාකමක් ඇත.මෙම සංයෝග සකස් කිරීම සඳහා අද්විතීය ප්රතික්රියා තත්වයන් අවශ්ය වේ, එබැවින් ඒවා සාමාන්ය පෙප්ටයිඩ සංශ්ලේෂණය කිරීමේදී බොහෝ විට භාවිතා නොවේ.
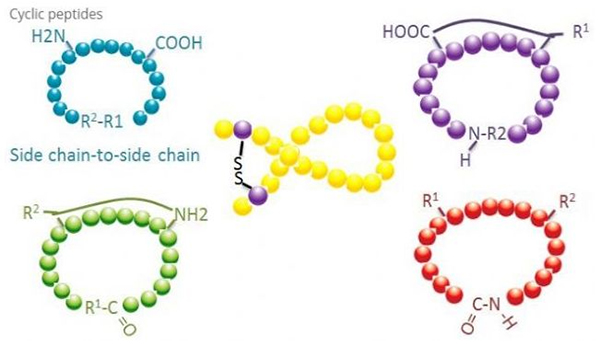
(2) පර්යන්තයේ සිට පැති දාමය
පර්යන්ත-පැති දාම චක්රීයකරණය සාමාන්යයෙන් ලයිසීන් හෝ ඕර්නිතින් පැති දාමයේ ඇමයිනෝ කාණ්ඩය සමඟ C-පර්යන්තය හෝ ඇස්පාර්ටික් අම්ලය හෝ ග්ලූටමික් අම්ලය පැති දාමය සහිත N-පර්යන්තය ඇතුළත් වේ.අනෙකුත් පොලිපෙප්ටයිඩ චක්රීයකරණය සිදු කරනු ලබන්නේ පර්යන්ත C සහ සෙරීන් හෝ ත්රෙයොනීන් පැති දාම අතර ඊතර් බන්ධන සෑදීමෙනි.
(3) පර්යන්ත හෝ හිස සිට වලිගය වර්ගය
දාම පොලිපෙප්ටයිඩ ද්රාවකයක චක්රීය කළ හැකිය, නැතහොත් පැති දාම චක්රීකරණය මගින් දුම්මල මත සවි කළ හැක.පෙප්ටයිඩවල ඔලිගොමරීකරණය වැළැක්වීම සඳහා ද්රාවක මධ්යගතකරණයේදී පෙප්ටයිඩ අඩු සාන්ද්රණයක් භාවිතා කළ යුතුය.හිස සිට වලිගය දක්වා කෘතිම මුදු පොලිපෙප්ටයිඩයක අස්වැන්න පොලිපෙප්ටයිඩ දාමයේ අනුපිළිවෙල මත රඳා පවතී.එබැවින්, මහා පරිමාණයෙන් චක්රීය පෙප්ටයිඩ සකස් කිරීමට පෙර, ප්රථමයෙන් දම්වැල් සහිත ඊයම් පෙප්ටයිඩ සහිත පුස්තකාලයක් නිර්මාණය කළ යුතු අතර, පසුව චක්රීයකරණයෙන් හොඳම ප්රතිඵල සහිත අනුපිළිවෙල සොයා ගත යුතුය.
2. N-methylation
N-methylation මුලින් ස්වභාවික පෙප්ටයිඩ වල සිදු වන අතර හයිඩ්රජන් බන්ධන ඇතිවීම වැලැක්වීම සඳහා පෙප්ටයිඩ සංස්ලේෂණයට හඳුන්වා දෙනු ලැබේ, එමගින් පෙප්ටයිඩ ජෛව හායනයට සහ නිෂ්කාශනයට වඩා ප්රතිරෝධී කරයි.N-methylated ඇමයිනෝ අම්ල ව්යුත්පන්නයන් භාවිතයෙන් පෙප්ටයිඩ සංශ්ලේෂණය වඩාත් වැදගත් ක්රමය වේ.මීට අමතරව, මෙතනෝල් සමඟ N-(2-nitrobenzene sulfonyl chloride) polypeptide-resin අතරමැදි වල Mitsunobu ප්රතික්රියාව ද භාවිතා කළ හැක.N-methylated ඇමයිනෝ අම්ල අඩංගු චක්රීය පෙප්ටයිඩ පුස්තකාල සකස් කිරීම සඳහා මෙම ක්රමය භාවිතා කර ඇත.
3. පොස්පරීකරණය
පොස්පරීකරණය යනු ස්වභාවධර්මයේ වඩාත් සුලභ පශ්චාත් පරිවර්තන වෙනස් කිරීම් වලින් එකකි.මිනිස් සෛල තුළ ප්රෝටීන වලින් 30% කට වඩා පොස්පරීකරණය වී ඇත.පොස්පරීකරණය, විශේෂයෙන් ප්රතිවර්ත කළ හැකි පොස්පරීකරණය, සංඥා සම්ප්රේෂණය, ජාන ප්රකාශනය, සෛල චක්රය සහ සයිටොස්කෙලිටන් නියාමනය සහ ඇපොප්ටෝසිස් වැනි බොහෝ සෛල ක්රියාවලීන් පාලනය කිරීමේදී වැදගත් කාර්යභාරයක් ඉටු කරයි.
විවිධ ඇමයිනෝ අම්ල අපද්රව්යවල පොස්පරීකරණය නිරීක්ෂණය කළ හැකි නමුත් වඩාත් පොදු පොස්පරීකරණය ඉලක්ක වන්නේ සෙරීන්, ත්රෙයොනීන් සහ ටයිරොසීන් අවශේෂ වේ.Phosfotyrosine, phosphothreonine සහ phosphoserine ව්යුත්පන්නයන් සංශ්ලේෂණය අතරතුර පෙප්ටයිඩවලට හඳුන්වා දිය හැකිය, නැතහොත් පෙප්ටයිඩ සංස්ලේෂණයෙන් පසුව සෑදිය හැක.ආරක්ෂිත කණ්ඩායම් තෝරා බේරා ඉවත් කරන සෙරීන්, ත්රෙයොනීන් සහ ටයිරොසීන් වල අපද්රව්ය භාවිතයෙන් වරණීය පොස්පරීකරණය ලබා ගත හැක.සමහර පොස්පරීකරණ ප්රතික්රියාකාරක වලට පසු වෙනස් කිරීම මගින් පොස්පරික් අම්ල කාණ්ඩ පොලිපෙප්ටයිඩයට හඳුන්වා දිය හැක.මෑත වසරවලදී, රසායනිකව තෝරාගත් ස්ටැඩිංගර්-පොස්ෆයිට් ප්රතික්රියාවක් භාවිතයෙන් ලයිසීන් හි අඩවි-විශේෂිත පොස්පරීකරණය සාක්ෂාත් කර ගෙන ඇත (රූපය 3).
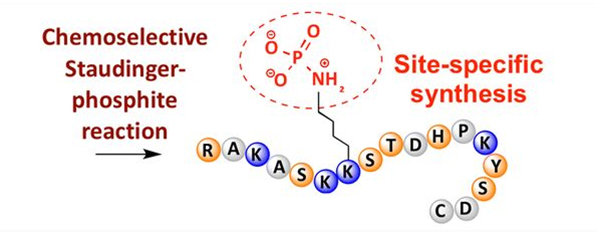
4. Myristoylation සහ palmitoylation
මේද අම්ල සමඟ N-පර්යන්තයේ ඇසිලේෂන් පෙප්ටයිඩ හෝ ප්රෝටීන සෛල පටල වලට බන්ධනය වීමට ඉඩ සලසයි.N-පර්යන්තයේ ඇති myridamoylated අනුක්රමය මගින් Src පවුලේ ප්රෝටීන් කයිනේස් සහ ප්රතිලෝම ට්රාන්ස්ක්රිප්ටේස් Gaq ප්රෝටීන සෛල පටලවලට බන්ධනය කිරීමට ඉලක්ක කර ගැනීමට හැකියාව ලැබේ.Myristic අම්ලය සම්මත සම්බන්ධක ප්රතික්රියා භාවිතයෙන් දුම්මල-පොලිපෙප්ටයිඩයේ N-පර්යන්තයට සම්බන්ධ කර ඇති අතර, එහි ප්රතිඵලයක් ලෙස ලිපොපෙප්ටයිඩය සම්මත තත්ව යටතේ විඝටනය කර RP-HPLC මගින් පිරිසිදු කළ හැක.
5. ග්ලයිකෝසිලේෂන්
vancomycin සහ teicolanin වැනි Glycopeptides මත්ද්රව්ය-ප්රතිරෝධී බැක්ටීරියා ආසාදනවලට ප්රතිකාර කිරීම සඳහා වැදගත් ප්රතිජීවක වන අතර ප්රතිශක්තිකරණ පද්ධතිය උත්තේජනය කිරීමට අනෙකුත් glycopeptides බොහෝ විට භාවිතා වේ.මීට අමතරව, බොහෝ ක්ෂුද්රජීවී ප්රතිදේහජනක ග්ලයිකෝසිලේටඩ් බැවින්, ආසාදනයේ චිකිත්සක බලපෑම වැඩි දියුණු කිරීම සඳහා ග්ලයිකොපෙප්ටයිඩ අධ්යයනය කිරීම ඉතා වැදගත් වේ.අනෙක් අතට, පිළිකා සෛලවල සෛල පටලයේ ඇති ප්රෝටීන අසාමාන්ය ග්ලයිකෝසයිලේෂන් ප්රදර්ශනය කරන බව සොයාගෙන ඇති අතර එමඟින් පිළිකා සහ පිළිකා ප්රතිශක්තිකරණ ආරක්ෂණ පර්යේෂණ සඳහා ග්ලයිකොපෙප්ටයිඩ වැදගත් කාර්යභාරයක් ඉටු කරයි.Glycopeptides සකස් කරනු ලබන්නේ Fmoc/t-Bu ක්රමය මගිනි.Glycosylated ඇමයිනෝ අම්ල ආරක්ෂා කිරීම සඳහා pentafluorophenol ester activated fMOCs මගින් threonine සහ serine වැනි Glycosylated අවශේෂ බොහෝ විට polypeptides වෙත හඳුන්වා දෙනු ලැබේ.
6. අයිසොප්රීන්
C-පර්යන්තය අසල පැති දාමයේ ඇති cysteine අවශේෂ මත Isopentadienylation සිදු වේ.ප්රෝටීන් අයිසොප්රීන් මගින් සෛල පටල සම්බන්ධය වැඩි දියුණු කළ හැකි අතර ප්රෝටීන්-ප්රෝටීන් අන්තර්ක්රියා ඇති කරයි.Isopentadienated ප්රෝටීන වලට tyrosine phosphatase, small GTase, cochaperone අණු, න්යෂ්ටික ලැමිනා සහ centromeric බන්ධන ප්රෝටීන ඇතුළත් වේ.අයිසොප්රීන් පොලිපෙප්ටයිඩ දුම්මල මත අයිසොප්රීන් භාවිතයෙන් හෝ සිස්ටීන් ව්යුත්පන්නයන් හඳුන්වා දීමෙන් සකස් කළ හැක.
7. පොලිඑතිලීන් ග්ලයිකෝල් (PEG) වෙනස් කිරීම
ප්රෝටීන් ජලවිච්ඡේදක ස්ථායීතාවය, ජෛව ව්යාප්තිය සහ පෙප්ටයිඩ ද්රාව්යතාව වැඩි දියුණු කිරීම සඳහා PEG වෙනස් කිරීම භාවිතා කළ හැක.පෙප්ටයිඩවලට PEG දාම හඳුන්වා දීමෙන් ඒවායේ ඖෂධීය ගුණ වැඩි දියුණු කළ හැකි අතර ප්රෝටියෝලයිටික් එන්සයිම මගින් පෙප්ටයිඩවල ජල විච්ඡේදනය ද වළක්වයි.PEG පෙප්ටයිඩ සාමාන්ය පෙප්ටයිඩ වලට වඩා පහසුවෙන් ග්ලෝමියුලර් කේශනාලිකා හරස්කඩ හරහා ගමන් කරයි, වකුගඩු නිෂ්කාශනය බෙහෙවින් අඩු කරයි.vivo හි PEG පෙප්ටයිඩවල දිගුකාලීන ක්රියාකාරී අර්ධ ආයු කාලය හේතුවෙන්, අඩු මාත්රාවලින් සහ අඩු නිතර පෙප්ටයිඩ ඖෂධ සමඟ සාමාන්ය ප්රතිකාර මට්ටම පවත්වා ගත හැක.කෙසේ වෙතත්, PEG වෙනස් කිරීම ද ඍණාත්මක බලපෑම් ඇති කරයි.PEG විශාල ප්රමාණයක් මගින් එන්සයිමය පෙප්ටයිඩ දිරාපත් වීම වළක්වන අතර ඉලක්ක ප්රතිග්රාහකයට පෙප්ටයිඩ බැඳීම අඩු කරයි.නමුත් PEG පෙප්ටයිඩවල අඩු සම්බන්ධය සාමාන්යයෙන් ඒවායේ දිගු ඖෂධීය අර්ධ ආයු කාලය මගින් සමනය වන අතර, වැඩි කාලයක් සිරුරේ පැවතීමෙන්, PEG පෙප්ටයිඩ ඉලක්ක පටකවලට අවශෝෂණය වීමේ වැඩි සම්භාවිතාවක් ඇත.එබැවින්, ප්රශස්ත ප්රතිඵල සඳහා PEG පොලිමර් පිරිවිතර ප්රශස්ත කළ යුතුය.අනෙක් අතට, වකුගඩු නිෂ්කාශනය අඩු වීම හේතුවෙන් PEG පෙප්ටයිඩ අක්මාව තුළ එකතු වන අතර, එහි ප්රතිඵලයක් ලෙස macromolecular syndrome ඇති වේ.එබැවින්, ඖෂධ පරීක්ෂණ සඳහා පෙප්ටයිඩ භාවිතා කරන විට PEG වෙනස් කිරීම් වඩාත් ප්රවේශමෙන් සැලසුම් කළ යුතුය.
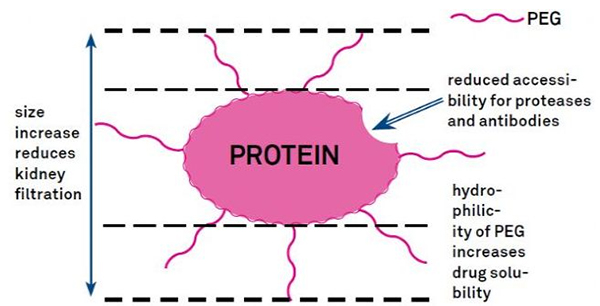
PEG විකරණකාරකවල පොදු වෙනස් කිරීමේ කණ්ඩායම් දළ වශයෙන් පහත පරිදි සාරාංශ කළ හැක: ඇමයිනෝ (-ඇමයින්) -NH2, aminomethyl-Ch2-NH2, hydroxy-OH, carboxy-Cooh, sulfhydryl (-Thiol) -SH, Maleimide -MAL, succinimide කාබනේට් - SC, succinimide acetate -SCM, succinimide propionate -SPA, n-hydroxysuccinimide -NHS, Acrylate-ch2ch2cooh, aldehyde -CHO (propional-ald, butyrALD වැනි), acrylic Base (-acrylate-acrl) Biotin, Fluorescein, glutaryl -GA, Acrylate Hydrazide, alkyne-alkyne, p-toluenesulfonate -OTs, succinimide succinate -SS, ආදිය. කාබොක්සිලික් අම්ල සහිත PEG ව්යුත්පන්නයන් n-terminal amines හෝ lysine chains සමඟ සම්බන්ධ කළ හැක.ඇමයිනෝ-ක්රියාකාරී PEG ඇස්පාර්ටික් අම්ලය හෝ ග්ලූටමික් අම්ලය පැති දාම සමඟ සම්බන්ධ කළ හැක.Mal-සක්රිය PEG සම්පුර්ණයෙන් ආරක්ෂා කරන ලද cysteine පැති දාම වල mercaptan වෙත සංකලනය කළ හැක [11].PEG විකරණකාරක සාමාන්යයෙන් පහත පරිදි වර්ගීකරණය කර ඇත (සටහන: mPEG යනු methoxy-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH) :
(1) සෘජු දාම PEG විකරණකාරකය
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) ද්වික්රියාකාරී PEG modifier
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) ශාඛා PEG විකරණකාරකය
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinization
Biotin avidin හෝ streptavidin සමඟ තදින් බැඳිය හැකි අතර, බන්ධන ශක්තිය සහසංයුජ බන්ධනයට පවා සමීප වේ.Biotin-labeled peptides බහුලව භාවිතා වන්නේ immunoassay, histocytochemistry සහ fluorescence-based flow cytometry වලය.බයෝටයිනයිලේටඩ් පෙප්ටයිඩ බන්ධනය කිරීමට ලේබල් කරන ලද ප්රතිජීවක ප්රතිදේහ ද භාවිතා කළ හැක.බයෝටින් ලේබල් බොහෝ විට ලයිසීන් පැති දාමයට හෝ N පර්යන්තයට අමුණා ඇත.6-aminocaproic අම්ලය බොහෝ විට peptides සහ biotin අතර බන්ධනයක් ලෙස භාවිතා වේ.බන්ධනය උපස්ථරයට බන්ධනය කිරීමේදී නම්යශීලී වන අතර ස්ටීරික් බාධාවක් ඇති විට වඩා හොඳින් බන්ධනය වේ.
9. ප්රතිදීප්ත ලේබල් කිරීම
සජීවී සෛලවල පොලිපෙප්ටයිඩ සොයා ගැනීමට සහ එන්සයිම සහ ක්රියාකාරී යාන්ත්රණ අධ්යයනය කිරීමට ප්රතිදීප්ත ලේබල් කිරීම භාවිතා කළ හැක.ට්රිප්ටෝෆාන් (Trp) ප්රතිදීප්ත වේ, එබැවින් එය ආවේණික ලේබල් කිරීම සඳහා භාවිතා කළ හැක.ට්රිප්ටෝෆාන් වල විමෝචන වර්ණාවලිය පර්යන්ත පරිසරය මත රඳා පවතින අතර ද්රාවක ධ්රැවීයතාව අඩු වීමත් සමඟ අඩු වේ, පෙප්ටයිඩ ව්යුහය සහ ප්රතිග්රාහක බන්ධනය හඳුනා ගැනීමට ප්රයෝජනවත් ගුණයකි.ප්රෝටෝන ඇස්පාර්ටික් අම්ලය සහ ග්ලූටමික් අම්ලය මගින් ට්රිප්ටෝෆාන් ප්රතිදීප්තතාව නිවාදැමිය හැකි අතර එමඟින් එහි භාවිතය සීමා කළ හැක.ඩැන්සිල් ක්ලෝරයිඩ් කාණ්ඩය (ඩැන්සිල්) ඇමයිනෝ කාණ්ඩයකට බැඳී ඇති විට ඉතා ප්රතිදීප්ත වන අතර බොහෝ විට ඇමයිනෝ අම්ල හෝ ප්රෝටීන සඳහා ප්රතිදීප්ත ලේබලයක් ලෙස භාවිතා කරයි.
ප්රතිදීප්ත අනුනාද බලශක්ති පරිවර්තනය (FRET) එන්සයිම අධ්යයනය සඳහා ප්රයෝජනවත් වේ.FRET යොදන විට, උපස්ථර පොලිපෙප්ටයිඩයේ සාමාන්යයෙන් ප්රතිදීප්ත-ලේබල් කිරීමේ කණ්ඩායමක් සහ ප්රතිදීප්ත නිවාදැමීමේ කණ්ඩායමක් අඩංගු වේ.ලේබල් කරන ලද ප්රතිදීප්ත කන්ඩායම් ෆෝටෝන නොවන බලශක්ති හුවමාරුව හරහා නිවාදැමීම මගින් නිවා දමනු ලැබේ.අදාළ එන්සයිමයෙන් පෙප්ටයිඩය විඝටනය වූ විට, ලේබල් කිරීමේ කණ්ඩායම ප්රතිදීප්ත විමෝචනය කරයි.
10. කූඩු පොලිපෙප්ටයිඩ
කූඩු පෙප්ටයිඩවල දෘශ්යමය වශයෙන් ඉවත් කළ හැකි ආරක්ෂිත කණ්ඩායම් ඇති අතර එය ප්රතිග්රාහකයට බන්ධනය වීමෙන් පෙප්ටයිඩ ආරක්ෂා කරයි.පාරජම්බුල කිරණවලට නිරාවරණය වන විට, පෙප්ටයිඩය සක්රිය කර, ප්රතිග්රාහකයට එහි සම්බන්ධතාවය නැවත ස්ථාපිත කරයි.මෙම දෘශ්ය සක්රිය කිරීම කාලය, විස්තාරය හෝ ස්ථානය අනුව පාලනය කළ හැකි නිසා, සෛල තුළ සිදුවන ප්රතික්රියා අධ්යයනය කිරීමට කූඩු පෙප්ටයිඩ භාවිතා කළ හැක.කූඩු පොලිපෙප්ටයිඩ සඳහා බහුලව භාවිතා වන ආරක්ෂිත කණ්ඩායම් වන්නේ 2-නයිට්රොබෙන්සයිල් කාණ්ඩ සහ ඒවායේ ව්යුත්පන්නයන් වන අතර ඒවා ආරක්ෂිත ඇමයිනෝ අම්ල ව්යුත්පන්නයන් හරහා පෙප්ටයිඩ සංස්ලේෂණයේදී හඳුන්වා දිය හැකිය.සංවර්ධනය කර ඇති ඇමයිනෝ අම්ල ව්යුත්පන්නයන් වන්නේ ලයිසීන්, සිස්ටීන්, සෙරීන් සහ ටයිරොසීන් ය.කෙසේ වෙතත්, ඇස්පාර්ටේට් සහ ග්ලූටමේට් ව්යුත්පන්නයන් පෙප්ටයිඩ සංස්ලේෂණය සහ විඝටනය අතරතුර චක්රීයකරණයට ඇති සංවේදීතාව නිසා බහුලව භාවිතා නොවේ.
11. Polyantogenic peptide (MAP)
කෙටි පෙප්ටයිඩ සාමාන්යයෙන් ප්රතිශක්තිකරණ නොවන අතර ප්රතිදේහ නිපදවීමට වාහක ප්රෝටීන සමඟ සම්බන්ධ කළ යුතුය.Polyantigenic peptide (MAP) සමන්විත වන්නේ ලයිසීන් න්යෂ්ටීන් හා සම්බන්ධ බහු අනන්ය පෙප්ටයිඩ වලින් වන අතර, ඒවාට විශේෂයෙන් ඉහළ ප්රබල ප්රතිශක්ති කාරක ප්රකාශ කළ හැකි අතර පෙප්ටයිඩ වාහක ප්රෝටීන යුගල සකස් කිරීමට භාවිතා කළ හැක.MAP පොලිපෙප්ටයිඩ MAP ෙරසින් මත ඝන අවධි සංස්ලේෂණය මගින් සංස්ලේෂණය කළ හැක.කෙසේ වෙතත්, අසම්පූර්ණ සම්බන්ධ කිරීම නිසා සමහර ශාඛාවල පෙප්ටයිඩ දාම අතුරුදහන් වීම හෝ කපා හැරීම සිදු වන අතර එම නිසා මුල් MAP පොලිපෙප්ටයිඩයේ ගුණාංග ප්රදර්ශනය නොවේ.විකල්පයක් ලෙස, පෙප්ටයිඩ වෙනම සකස් කර පිරිසිදු කර පසුව MAP එකට සම්බන්ධ කළ හැක.පෙප්ටයිඩ හරයට අමුණා ඇති පෙප්ටයිඩ අනුපිළිවෙල හොඳින් අර්ථ දක්වා ඇති අතර ස්කන්ධ වර්ණාවලීක්ෂය මගින් පහසුවෙන් සංලක්ෂිත වේ.
නිගමනය
පෙප්ටයිඩ වෙනස් කිරීම පෙප්ටයිඩ නිර්මාණය කිරීමේ වැදගත් මාධ්යයකි.රසායනිකව වෙනස් කරන ලද පෙප්ටයිඩ වලට ඉහළ ජීව විද්යාත්මක ක්රියාකාරකම් පවත්වා ගැනීමට පමණක් නොව, ප්රතිශක්තිකරණ හා විෂ සහිත දුර්වලතා ඵලදායී ලෙස වළක්වා ගත හැකිය.ඒ අතරම, රසායනික වෙනස් කිරීම් මගින් පෙප්ටයිඩවලට නව විශිෂ්ට ගුණාංග ලබා දිය හැකිය.මෑත වසරවලදී, පොලිපෙප්ටයිඩ පශ්චාත් වෙනස් කිරීම සඳහා CH සක්රිය කිරීමේ ක්රමය වේගයෙන් වර්ධනය වී ඇති අතර, බොහෝ වැදගත් ප්රතිඵල ලබා ගෙන ඇත.
පසු කාලය: මාර්තු-20-2023
